糖タンパク質の安定同位体標識

「Biomolecular NMR」カタログ(大陽日酸 2015) 寄稿文

加藤晃一
自然科学研究機構
岡崎統合バイオサイエンスセンター
教授
タンパク質の多くは裸の状態ではなく糖鎖という衣装を身に纏って働いている。自然界に存在するタンパク質全種類の実に半数以上は糖鎖による修飾をうけているものと見積もられている。糖鎖は、タンパク質の溶解性や熱安定性といった物理化学的性質を規定しているばかりでなく、タンパク質機能部位の構造構築に積極的に関わり、レクチンと総称されるタンパク質との相互作用を通じて、様々な生命現象を媒介している。例えば、糖鎖は細胞の顔としてその表層を覆い、
細胞同士のコミュニケーションにおける言語としての役割を演じており、その一方でウイルスが感染する際の標的にもなっている。タンパク質の細胞内外における運命もそれらが担う糖鎖とレクチンとの相互作用を通じて決定されている。特に最近は、創薬の分野で糖鎖の存在が注目されている。主要なバイオ医薬は糖タンパク質であり、その性状と性能に糖鎖の構造が深く関わっていることが明らかになってきているからである。例えば、代表的なバイオ医薬である抗体においては、そのFc領域に結合している糖鎖の構造のわずかな違いによってがん細胞を殺傷する能力が100倍近くも変わってくることが知られている。近年の構造生物学の進展によってタンパク質の立体構造情報は爆発的な勢いで蓄積されてきている。しかしながら、プロテインデータバンクに登録されているタンパク質3次元構造データ約10万件のうち
糖タンパク質に関するものは全体の4%にも満たず、NMRで決定されたものは20例以下(0.02%)に留まっている1)。しかもその大半はわずか糖1残基程度の情報を与えているにすぎない。構造生物学研究で広く用いられている大腸菌発現系や無細胞系で糖タンパク質を発現する方法が確立していないことがその大きな理由である。また、タンパク質を修飾する糖鎖の構造は化学的に不均一であるとともに高い柔軟性を有しているがゆえに結晶化が困難である。これらも糖鎖の構造生物学研究を阻んできた要因である。それゆえに、これまでの構造生物学は糖鎖の存在を無視して解析を行うということが往々にして行われてきた。(ちなみに、このような状況は構造生物学に限らず生体分子研究に広くみられてきた風潮で、glycophobics と言い表されるほどである。)
NMRは糖タンパク質のような動的不均一系の構造解析を可能とする潜在的能力を持っているが、その有用性を十分に発揮するためには試料に安定同位体標識を施すことが必要不可欠である。現在のところ糖タンパク質の安定同位体標識に最も有効な方法は真核細胞を利用したタンパク質発現系を利用することである。動物細胞、昆虫細胞、酵母など様々な真核細胞発現系を利用した標識技術がこれまでに報告されている2)。私たちは、大陽日酸の支援のもとで哺乳動物細胞発現系を用いた糖タンパク質の代謝標識技術の開発と応用に取り組んできた。例えば、バイオ医薬品の生産に広く用いられているチャイニーズハムスター卵巣(CHO)細胞を代謝前駆体(アミノ酸、グルコース、ピルビン酸、コハク酸)をすべて安定同位体標識体で置き換えた無血清培地中で培養することによって、均一に13Cおよび15N標識した抗体を調製することができる3)。ヒト抗体IgGのFc領域(分子質量53kDa)に関しては最近、主鎖シグナルの帰属を公開した4)。
こうした情報を利用することによって糖鎖改変やアミノ酸残基置換あるいは長期保存などに伴う抗体の構造変化を細やかに評価することが可能となり、抗体医薬の設計・開発にも役立つものと期待される。このように培養動物細胞を利用した糖タンパク質の安定同位体標識は少しずつ普及してきているが未だ生産コストが高いことが懸案材料であろう。私たちは、哺乳類細胞以外の真核生物発現系にも注目して糖タンパク質の安定同位体標識技術を開発することにも取り組んでいる。例えば、出芽酵母を利用したシステムは、糖鎖プロセシングに関わる遺伝子をノックアウトすることによって糖タンパク質の糖鎖構造を均一化した状態で同位体標識する技術へと発展しつつある(産総研糖鎖医工学研究センター千葉靖典先生らとの共同研究)5)。また、トランスジェニックタバコを硝酸カリウム、硝酸アンモニウムを主な窒素源として水耕栽培することによって15N標識した抗体を生産しNMR計測を実施している(産業技術総合研究所 北海道センター松村健先生らとの共同研究)6)。
ごく最近、生きたカイコにバキュロウイルスを感染させるシステムを利用して安定同位体標識した抗体を発現し、そのNMR解析に成功している7)。これは同位体標識した酵母から抽出したタンパク質を含む人工飼料を大陽日酸と共同で開発することによってはじめて実現されたものである。糖鎖の構造はゲノムに直接コードされていないため、その構造を自由自在にコントロールすることはこれからの課題だが、糖鎖の生合成に関わる遺伝子の導入や発現制御などを通じてタンパク質の糖鎖構造をテーラーメードなかたちで生産しようという試みも着実に進展しつつある。構造生物学がこれまで積極的に取り扱ってこなかった糖タンパク質もNMR解析として益々身近なものとなるに違いない。こうした技術は基礎研究のみならずバイオ医薬品の設計・開発や高度化をはじめとする産業界のニーズに応えることにもつながるであろう。
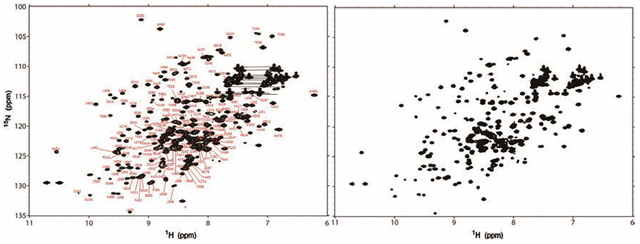
図 CHO細胞(左)およびカイコ(右)を用いて発現した抗体のFc領域の1H-15N HSQC スペクトル(文献4および7より引用)
参考文献
1)Y. Kamiya, T. Satoh, and K. Kato: Curr Opin Struct Biol, 26, 44-53 (2014)
2)K. Kato, Y. Yamaguchi, and Y. Arata: Progress in nuclear magnetic resonance spectroscopy, 56, 346-359 (2010)
3)Y. Yamaguchi, and K. Kato: Methods in enzymology, 478, 305-322 (2010)
4)H. Yagi, Y. Zhang, M. Yagi-Utsumi, T. Yamaguchi, S. Iida, Y. Yamaguchi, and K. Kato: Biomol. NMR assign., Oct. (2014) DOI 10.1007/s12104-014-9586-7
5)Y. Kamiya, S. Yamamoto, Y. Chiba, Y. Jigami, and K. Kato: J Biomol NMR, 50, 397-401 (2011)
6)H. Yagi, N. Fukuzawa, Y. Tasaka, K. Matsuo, Y. Zhang, T. Yamaguchi, S. Kondo, S. Nakazawa, N. Hashii, N. Kawasaki, T. Matsumura, and K. Kato: Plant Cell Reports, 34, 959-968 (2015)
7)H. Yagi, M. Nakamura, J. Yokoyama, Y. Zhang, T. Yamaguchi, S. Kondo, J. Kobayashi, T. Kato, Y. E. Park, S. Nakazawa, N. Hashii, N. Kawasaki, and K. Kato: J. Biomol. NMR, in press (2015) DOI 10.1007/s10858-015-9930-y


イノベーションユニット
SI事業部
045-872-1823
※月~金曜日
9:00~17:40
045-872-1825
Isotope.TNS@tn-sanso.co.jp
〒220-8561
神奈川県
横浜市西区
みなとみらい4-6-2
みなとみらい
グランドセントラルタワー 7F
大陽日酸㈱
みなとみらい事業所内

高圧ガス販売事業(第1種、第2種)
毒物劇物一般販売業 / 毒物劇物輸入業
医療をはじめ、研究から産業まで広くご利用いただける安定同位体試薬をご提供いたします。
Copyright © 2021. TAIYO NIPPON SANSO Corporation. All Rights Reserved.








